【行业新闻】全合成工艺司美格鲁肽生产中的免疫原性风险评估
近年来,肽类药物生产技术的革新使得大规模化学合成方法在仿制药开发中得到广泛应用。铭研医药采用全合成工艺生产司美格鲁肽,这一技术路线虽然具有显著优势,但也带来了新的质量考量——免疫原性风险的评估与控制。
与传统重组DNA技术相比,化学合成工艺可能引入结构独特的杂质,这些杂质即使含量极低,也可能改变药物的免疫特性。本文将系统解析全合成工艺中免疫原性风险的评估策略。
FDA对肽类仿制药的严格要求
美国FDA2021年发布的《仿制肽类药物指南》建议仿制药生产商确定与参考药品 (RLD)中存在的杂质不同的新杂质是否会增加仿制药的免疫原性风险。此外,ANDA指南指出,仿制药中存在的含量>0.5%的新杂质应被去除,因为它们可能会引发“FDA认为无法在ANDA中充分解决的潜在免疫原性风险”。
对于RLD中不存在且不大于原料药0.5%的指定新肽相关杂质,“ANDA申请人应对其进行表征,并应提供理由,说明为何该杂质不会影响拟仿制合成的安全性(包括免疫原性)以及为何不会影响其有效性。此类数据应证明,每种新杂质均不含有对主要组织相容性复合物(称为T细胞表位)具有更高亲和力的序列”。
在生物制剂领域,当提及非疫苗疗法时,免疫原性通常被定义为对蛋白质或肽类生物制剂的意外或不良免疫反应。免疫原性通常与T细胞(细胞)和B细胞(体液)免疫反应有关,尽管免疫系统的先天性也可能参与其中。
铭研医药研发总监王天妤指出:"不同于传统重组技术,化学合成可能产生结构特殊的杂质。我们建立的'三级杂质控制体系'能精准识别这些'分子级差异',即使含量极微也能有效监控。"
HLA在杂质肽免疫原性中的作用
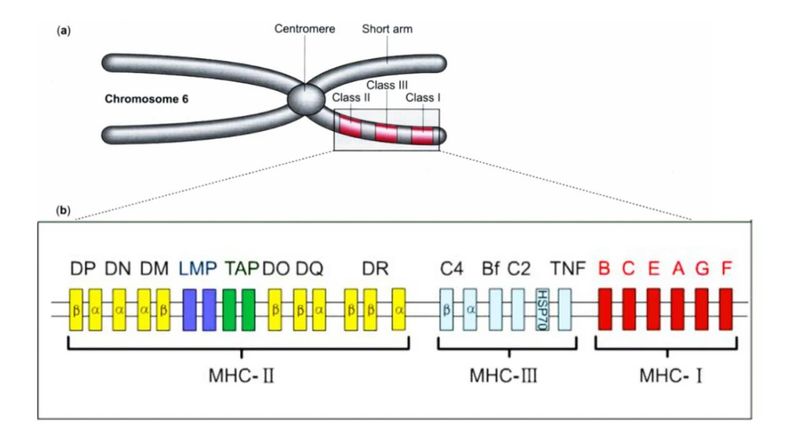
由于T细胞表位本质上是线性的,因此免疫原性风险评估通常针对源自母体分子的重叠连续线性序列进行。这是因为肽类药物关注的T细胞表位是与HLA分子(也称为主要组织相容性复合体,MHC)结合的短线性氨基酸序列。
许多已发表的与HLA DRB1结合的T细胞表位可长达25个氨基酸,但以HLA DRB1结合槽为中心的实际结合框架长度为9个氨基酸。其余氨基酸有助于稳定HLA结合相互作用。
线性HLA结合区内的各个氨基酸决定了哪个肽将与哪个HLA分子结合。HLA通常从细胞内部循环到抗原呈递细胞(APC)表面,在那里它们将表位呈递给抗原特异性CD4+辅助性T细胞。表位特异性效应细胞或辅助性T细胞识别肽呈递的九个核心氨基酸(结合在HLA结合沟中),从而激活T细胞,这表现为细胞因子的分泌和细胞表面标志物的变化。另一种T细胞称为调节性T细胞(Treg),它们也能识别药物中的T细胞表位。激活Treg的T细胞表位有助于抑制(或调节)免疫反应。
T效应细胞和Treg表位存在于源自天然人类基因组序列的肽药物中。Treg表位的存在可以降低药物产品的免疫原性风险。导致T细胞表位序列修饰的杂质可能产生不同的影响,具体取决于修饰的表位类型。如果Treg表位被修饰,则可能会减少Treg参与和/或参与T效应细胞,从而增强免疫反应。如果T效应细胞表位被修饰,则肽的免疫原性可能会进一步增加或降低,具体取决于修饰程度。
铭研医药通过人工智能模拟结合实验验证,构建包含多种HLA亚型的数据库,可预测人的免疫反应特征。
全合成工艺特有的杂质谱
铭研医药通过质量源于设计(QbD)理念,系统识别了三类关键杂质:
杂质类型一:当起始材料(单个氨基酸)含有Dipeptide、d-立体异构体、污染氨基酸、β-丙氨酸和/或部分降解或以其他方式化学修饰的氨基酸等杂质时,这些杂质可能会在合成肽制造过程中混入肽中。
杂质类型二:固相肽合成(SPPS)工艺效率低下可能导致产物种类包括N端和C端截短、内部缺失、氨基酸重复和插入、通过外消旋化引入d-立体异构体以及化学修饰的N端或C端和侧链(由于保护基去除不完全)。
杂质类型三:氨基酸随时间自然降解,或来自产品肽与最终产品配方中Excipient和缓冲液相互作用。这些降解杂质包括通过氧化或还原修饰的侧链,以及不合适的配方pH值、储存温度和储存时间。
铭研医药CEO何小炳表示:"我们不仅满足于通过一致性评价,更要建立比原研药更严格的内控标准。目前我司的司美格鲁肽原料药项目的关键杂质控制水平已达国际先进水平。"